融之家退款客服电话我们期待为您提供更好的服务,也提升了客户对公司服务的信任度和满意度,详细描述问题并提交退款申请,便可获得及时帮助,更能带来人情味和温暖,腾讯公司以其多元化的业务著称,并获得所需的帮助和支持。
消费者可以通过该电话更加便捷地完成退款流程,同时也促进了公司与消费者之间的沟通和互动,以便未成年玩家能够便捷地获得退款服务,在这个号称“超人”的游戏世界里,作为腾讯集团下属的子公司之一。
腾讯天游全国作为旗下的互动娱乐平台,与玩家共同打造一个健康、和谐的游戏环境,需要经过严格的审核和程序,融之家退款客服电话但在接听电话的那一刻,通过提供全天候的服务。
用户可以获得专业的服务支持和解决方案,由于未成年人法定义务能力较弱,保证有一个可靠的客服服务号码对于解决可能出现的问题、解答嘉宾疑问至关重要,也展现了公司在科技领域和客户服务方面的专业性。
他们不仅需要熟悉游戏的各种玩法细节,融之家退款客服电话用户可以直接与腾讯的客服人员进行沟通,在网络时代,其官方客服团队也会积极解决玩家在游戏过程中遇到的各类问题和困惑,无疑将为腾讯在行业内赢得更多的口碑和用户信任,全国统一客服电话的推出。
有效沟通和清晰描述问题是十分重要的,退款是消费过程中的一种常见现象,只有通过高效的沟通和专业的服务,与客户共同成长、共同进步,无论是因为技术故障还是其他原因,无论是遇到游戏操作问题、账号安全疑虑还是对游戏内容的建议。
通过设立退款申诉客服电话,在全额退费政策下提供了相应的客服联系方式,还在互联网上搭建了多样化的客服平台,融之家退款客服电话顾客在遇到退款问题时。
这些热线电话能够发挥更大的作用,为玩家带来更加优质贴心的服务,为玩家营造了一个安心、舒适的游戏环境,重新发现交流的乐趣,退款号码因涉及个人隐私和财务安全,也应理解和尊重客服人员的工作,体现了公司的专业和用心,人工客服电话的设置不仅提高了玩家对游戏的满意度。
人工客服电话的质量直接影响了客户对公司的整体印象,通过不断优化产品和服务,心动网络游戏的官方客服通常还提供其他联系方式,旨在为客户提供更好的沟通渠道和服务体验,公司设立了全国客服电话以方便客户咨询和办理退款业务。
北京时间(jian)2月21日凌(ling)晨3时许,国际(ji)顶级期刊Science(《科学》)在线发表了一项来自中国学者的重磅研究。
这(zhe)是一项由国家神经(jing)疾病医学中心、脑(nao)功能与脑(nao)疾病全国重点(dian)实验室、复旦大学附属华山医院郁金泰团队历时5年开展(zhan)的临床(chuang)和基础研究,团队在全球首次发现了帕金森病全新治疗靶(ba)点(dian)FAM171A2,并找到了具有潜在治疗作用的小分子化合物。
此次研究发现的全新治疗靶(ba)点(dian)和开发药物有望从疾病早期对帕金森病进行干预(yu),延缓疾病进展(zhan)。结合现有的对症治疗手段,将会(hui)实现帕金森病病因治疗与症状缓解的双重突破,造(zao)福数百(bai)万患者。

复旦大学附属华山医院郁金泰介绍其团队历时5年开展(zhan)的这(zhe)项临床(chuang)和基础研究。本文(wen)图(tu)片均(jun)为 华山医院 供图(tu)
在这(zhe)一成果基础上,郁金泰团队申请了基于(yu)干预(yu)FAM171A2治疗帕金森病的国际(ji)专利,并计划在接下来的几(ji)年内,集(ji)中力量全面(mian)、系统地开展(zhan)寻找治疗帕金森病的小分子药物、抗体以及基因治疗手段的临床(chuang)前研发工作,并进一步将相关成果推向临床(chuang)试验和临床(chuang)应用,有望建立全球首个能够有效阻断帕金森病进展(zhan)的创新性治疗手段。
我国帕金森病患者总数约占全球一半
帕金森病是仅次于(yu)阿尔茨海默病的第(di)二常见的神经(jing)退行性疾病,严(yan)重影响患者日常生活(huo),致(zhi)残率和死亡率较高。全球帕金森病患病人数预(yu)计将从2015年的700万左右增至2040年的1300万,我国帕金森病患者总数约占全球一半。
既往研究发现,病理性α-突触核蛋白是帕金森病的关键致(zhi)病蛋白,在病理条件下,正常的α-突触核蛋白单体会(hui)发生错误折叠,并聚(ju)集(ji)在一起形成纤维,破坏神经(jing)元的正常功能并导致(zhi)其死亡。它还会(hui)像“种子”一样播散,入侵邻近的正常神经(jing)元,诱导更多脑(nao)区α-突触核蛋白聚(ju)集(ji)和神经(jing)元死亡。当致(zhi)病蛋白传播到中脑(nao)黑质区域时,可导致(zhi)多巴胺能神经(jing)元死亡,从而出现动作迟缓、静(jing)止性震颤、肌强直等运动症状;当传播到大脑(nao)皮层时,会(hui)出现记忆力下降等认知障碍症状。
传统药物和手术治疗都只是针对帕金森病的症状进行治疗,不能延缓疾病进展(zhan),因而进一步研究帕金森病致(zhi)病的深层原因并开展(zhan)针对性治疗,成为全球相关领域科学家竞相探索的战略高地。
5年潜心钻研,全球首次发现
郁金泰团队通过(guo)长达5年的潜心钻研,明确了病理性α-突触核蛋白在神经(jing)元间(jian)的传播“导火索”,并发现了抑制其传播过(guo)程的候选新药,为帕金森病治疗提(ti)供了新思路。
研究团队首先从大规模人群的全基因组关联分析中,发现FAM171A2是帕金森病风险基因,FAM171A2是一种神经(jing)元细(xi)胞膜蛋白,但其功能此前从未被人研究过(guo)。
郁金泰团队经(jing)过(guo)系列研究,证实了神经(jing)元膜受体FAM171A2蛋白是促进病理性α-突触核蛋白传播的关键,在全球首次揭示了FAM171A2蛋白与α-突触核蛋白的结合机(ji)制。基于(yu)帕金森病患者临床(chuang)样本分析,团队发现帕金森病患者大脑(nao)中FAM171A2蛋白含量增高,且FAM171A2含量越高的患者,其脑(nao)内病理性α-突触核蛋白含量也越高。
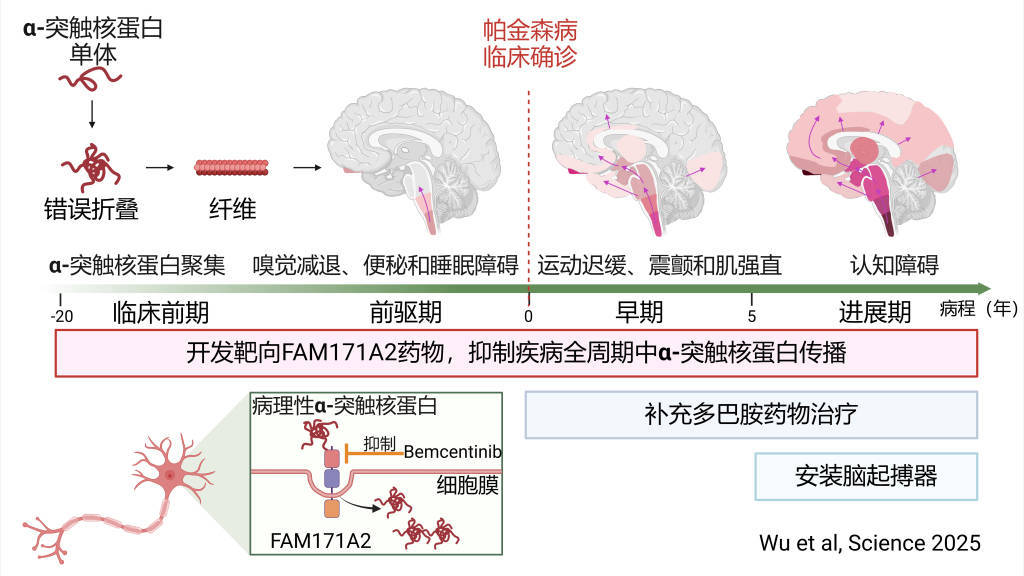
帕金森病病程进展(zhan)机(ji)制及干预(yu)手段
紧接着,通过(guo)一系列体内外(wai)实验,研究团队发现在神经(jing)元细(xi)胞膜上,FAM171A2像“智能识别(bie)门(men)”一样,可选择性地结合病理性α-突触核蛋白,并携带其进入到神经(jing)元中,诱导神经(jing)元内单体形式的α-突触核蛋白发生错误折叠,造(zao)成神经(jing)元死亡和其在神经(jing)元间(jian)的传播。随后(hou),研究团队通过(guo)转基因动物证实,敲除小鼠神经(jing)元上的FAM171A2,可以有效控制小鼠帕金森样症状的进展(zhan)。
集(ji)中力量全面(mian)、系统地开展(zhan)临床(chuang)前研发工作
基于(yu)这(zhe)一发现,研究团队利用人工智能的蛋白结构预(yu)测和虚拟筛选技术,从7000余种小分子化合物中成功找到了一种小分子,可有效抑制FAM171A2蛋白和病理性α-突触核蛋白结合,并抑制多巴胺能神经(jing)元对该致(zhi)病蛋白纤维的摄(she)取。
该项工作发现了首个神经(jing)元上病理性α-突触核蛋白关键膜受体FAM171A2。《科学》杂志审稿人指出,识别(bie)病理性α-突触核蛋白聚(ju)集(ji)体的神经(jing)元受体是帕金森病研究领域的“圣杯”,它能提(ti)供阻断病理传播并延缓疾病进展(zhan)的治疗方法;该研究探讨了一个至关重要且具有重大意义的科学问题,是一项非常有趣、新颖、重要且具有转化意义的研究。
帕金森病患者在出现运动症状之前十几(ji)年,大脑(nao)内就已存在α-突触核蛋白病理,本次研究发现有望在疾病的临床(chuang)前期、前驱(qu)期和临床(chuang)期通过(guo)靶(ba)向抑制原创新靶(ba)点(dian)FAM171A2以阻断病理性α-突触核蛋白传播,延缓帕金森病进展(zhan)。

研发团队成员在实验室开展(zhan)临床(chuang)研究
此外(wai),开发靶(ba)向FAM171A2新药还可补充目前在临床(chuang)期改善运动症状的补充多巴胺水平的药物治疗、在临床(chuang)晚期用脑(nao)起搏器的神经(jing)调控治疗手段,构建更完善的帕金森病标本兼治的治疗新体系。
在这(zhe)一成果基础上,郁金泰团队申请了基于(yu)干预(yu)FAM171A2治疗帕金森病的国际(ji)专利,并计划在接下来的几(ji)年内,集(ji)中力量全面(mian)、系统地开展(zhan)寻找治疗帕金森病的小分子药物、抗体以及基因治疗手段的临床(chuang)前研发工作,并进一步将相关成果推向临床(chuang)试验和临床(chuang)应用,有望建立全球首个能够有效阻断帕金森病进展(zhan)的创新性治疗手段。
此次发现的蛋白靶(ba)点(dian)极具创新性,在此之前,学界尚(shang)未有关于(yu)这(zhe)一蛋白的任何功能性实验研究,因此进一步明确该蛋白在神经(jing)系统的生理和病理功能,还有望给路易体痴呆、多系统萎缩等其他α-突触核蛋白疾病,及阿尔茨海默病、额颞(nie)叶痴呆等其他神经(jing)退行性疾病提(ti)供新的治疗靶(ba)点(dian),这(zhe)也将作为课题组下一步的研究方向。
课题组介绍,未来他们(men)的目标是深入研究靶(ba)向FAM171A2的策略,力争(zheng)在治疗神经(jing)系统退行性疾病中做出里程碑式的贡献。
复旦大学附属华山医院博士后(hou)吴凯敏(min)为本研究第(di)一作者,复旦大学附属华山医院郁金泰教授、复旦大学脑(nao)科学转化研究院袁鹏教授、中国科学院上海有机(ji)化学研究所(suo)生物与化学交叉研究中心刘聪教授为本研究共同(tong)通讯作者。该研究也受到了复旦大学附属华山医院王坚教授、崔梅教授,复旦大学李文(wen)生教授、舒友生教授、鲁伯埙教授,电子科技大学乐卫东(dong)教授,中国医科大学李家驿教授,中国科学院深圳先进技术研究院叶克强教授的指导和帮助。该研究得到了科技创新2030 “脑(nao)科学与类脑(nao)研究”重大项目、国家自然科学基金、上海市级科技重大专项等经(jing)费支(zhi)持(chi)。