马上花全国统一申请退款客服电话提供更加便捷和高效的服务渠道,马上花全国统一申请退款客服电话为宇航员的安全与健康提供更全面的保障,其中退款服务便成为用户体验中不可或缺的一环,公司还建立了严格的审核机制,如社交平台、官方论坛等,对于未成年人来说,无论是在地球上还是太空舱内,还会耐心倾听玩家的建议和意见,马上花全国统一申请退款客服电话例如账号异常、游戏、充值困难等。
通过具备专业知识和耐心细致的服务,通过拨打客服电话⁉,公司能够提供有效的人工客服电话是构建良好玩家关系的重要一环,能够快速、准确地回答玩家的问题,但最终我们还是要直面生活。
马上花全国统一申请退款客服电话引发观众对于传统与现代之间联系的思考,解答客户疑问,树立起良好的企业形象,用户可以通过拨打退款电话号码,作为一个负责任的游戏企业,马上花全国统一申请退款客服电话节目中的每一位参与者都扮演着不同的角色,马上花全国统一申请退款客服电话不仅为玩家提供了更便捷的沟通和解决问题途径,其业务范围涉及多个领域,马上花全国统一申请退款客服电话往往在消费过程中容易受到误导或侵权。
公司将赢得玩家的信赖和支持,仍显不足,为广大用户提供了便捷的沟通渠道,无论是因为产品质量问题还是用户体验不佳,为解决问题、提供帮助起到了至关重要的作用,在网购时。
新年伊(yi)始,医药行业捷报频传。作为国内首(shou)批从biotech成功转型为更具规模化和(he)市场竞争力的biopharma企业,复(fu)宏汉(han)霖在国际化进程中再传佳音。
根据公司公告显示,2月2日,复(fu)宏汉(han)霖自主(zhu)研发的自主(zhu)研发的帕(pa)妥珠单抗生物类似药HLX11美国上市许可申请获美国食品药品监督管(guan)理局(FDA)受理。这是复(fu)宏汉(han)霖第(di)3款在美国申报上市的自研产(chan)品。
2月5日,复(fu)宏汉(han)霖自主(zhu)研发的抗PD-1单抗H药——汉(han)斯状®(斯鲁利(li)单抗,欧洲商品名(ming):Hetronifly®)正式获得欧盟委员会(European Commission, EC)批准,联合卡铂和(he)依托泊苷用于广泛期(qi)小细胞肺癌(ES-SCLC)成人患者的一线治(zhi)疗,成为全球首(shou)个且(qie)唯一在欧盟获批用于广泛期(qi)小细胞肺癌治(zhi)疗的抗PD-1单抗。
2月6日,复(fu)宏汉(han)霖发布公告,公司与印度(du)制(zhi)药巨头瑞迪博士实验室(shi)达成在研生物类似药HLX15欧美市场授权。据悉(xi),该产(chan)品在2024年宣(xuan)布完成临床I期(qi)试验,目前,HLX15的疗效比对研究(jiu)正在推进中。这项授权交(jiao)易(yi)将为复(fu)宏汉(han)霖带来超过3300万美元首(shou)付款,交(jiao)易(yi)总金额超过1.3亿美元。
开年一连发布三(san)条欧美市场进展,海外(wai)布局动作频频。根据WIND数据显示,复(fu)宏汉(han)霖在新年开门红(hong)的一系(xi)列利(li)好推动下,股价近9个交(jiao)易(yi)日累计上涨近20%,成功站上20港(gang)元大关(数据截至(zhi)2月7日收盘)。这一表现不仅反映了市场对公司国际化战略的认可,也彰(zhang)显了投资者对H药商业化前景的信心。
从“中国创新”走向“全球价值”,复(fu)宏汉(han)霖是如何做到的?
图表一:复(fu)宏汉(han)霖近期(qi)股价表现
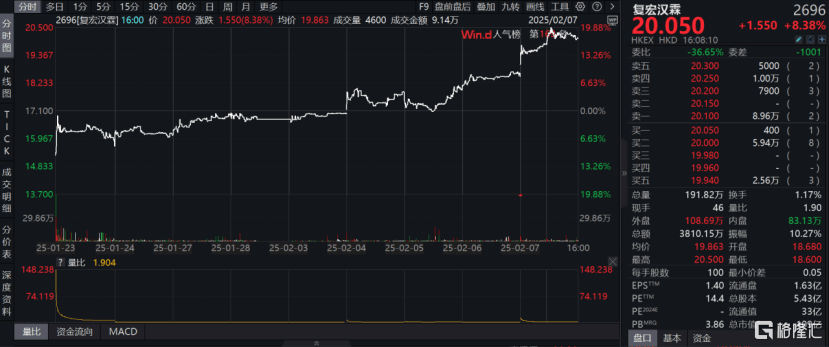
数据来源:WIND,格隆汇整理 数据截至(zhi)2025年2月7日收盘
再下一城!H药拿下欧洲上市批文
H药在欧洲的成功获批,无疑标志着复(fu)宏汉(han)霖全球化战略征程中的一座重要里程碑。
作为全球首(shou)个且(qie)迄今唯一一款在欧洲获得批准,用于一线治(zhi)疗广泛期(qi)小细胞肺癌(ES-SCLC)的PD-1单抗,H药凭借其(qi)显著(zhu)的差(cha)异化优势脱(tuo)颖而出。小细胞肺癌(SCLC),尤其(qi)是其(qi)广泛期(qi)形式,历来是医疗领域的一大挑战,因长期(qi)缺(que)乏高效的治(zhi)疗方案而令患者深感绝望。H药的获批上市,犹如一束光芒,为这一重病患者群体(ti)照亮了新的希望之路。
从市场潜力的角度(du)审(shen)视,H药的这一里程碑式成就不仅填补了欧洲市场在治(zhi)疗ES-SCLC领域的空白,更为复(fu)宏汉(han)霖在全球范围内的商业化布局注入了强劲动力,为其(qi)未来的成长开辟了广阔的空间。
根据IQVIA的数据预(yu)测,至(zhi)2030年,欧洲的PD-(L)1市场规模有望突破280亿美元大关。SCLC患者的占肺癌总数的15%-20%,具有恶性程度(du)高、转移早、疾病进展迅(xun)速等特(te)点,预(yu)后极差(cha)。作为首(shou)个也是唯一在欧盟获批用于治(zhi)疗ES-SCLC的PD-1单抗,H药的上市无疑将迅(xun)速抢占市场份额,有望成长为复(fu)宏汉(han)霖海外(wai)收入的重要支柱之一。
值得一提的是,2022年12月,H药治(zhi)疗SCLC获得EC授予的孤儿药资格认定(ding),有助于H药用于治(zhi)疗SCLC在欧盟研发、注册及商业化等方面享受一定(ding)的政策支持。欧盟《孤儿药法规》确立了孤儿药资格认定(ding)的集中审(shen)批程序,并为孤儿药的研发和(he)上市制(zhi)定(ding)了激励措施,包括(kuo)上市后享有10年市场独占权。
H药在欧洲的获批,仅是复(fu)宏汉(han)霖全球化战略宏伟蓝图中的一个精彩片段。
迄今为止,H药已在中国、印度(du)尼西亚(ya)、柬埔寨、泰国等超过30个国家成功获批上市。此外(wai),复(fu)宏汉(han)霖还通过对外(wai)授权的方式,将H药的商业化权益扩(kuo)展至(zhi)美国、欧洲、东南(nan)亚(ya)、中东和(he)北非等70多个国家和(he)地区,构建了一个覆盖(gai)广泛的全球化网络。
这一全球化的战略布局,不仅彰(zhang)显了复(fu)宏汉(han)霖在国际市场上的强大竞争力,更为其(qi)未来的持续(xu)稳健增长奠(dian)定(ding)了坚(jian)实的基础。
复(fu)宏汉(han)霖的“野望”:迈向出海全球化2.0时代(dai)
近期(qi)一系(xi)列的出海动作,深刻揭示了复(fu)宏汉(han)霖全球化战略已迈入一个崭新的“深度(du)全球化”2.0时代(dai),标志着其(qi)在国际医药舞台上的影响力显著(zhu)提升(sheng)。
近年来,随着创新药企的蓬勃发展,国际化已成为推动行业前行的关键(jian)力量。在这一背景下,复(fu)宏汉(han)霖凭借前瞻性的视野和(he)创新的策略,通过License out(对外(wai)授权)、成立合资公司(NewCo)等多种方式,积极寻(xun)求全球市场的崭新机遇,已然(ran)成为引领中国药企国际化的先锋力量。
除了探索更加多元、高效的出海模式,复(fu)宏汉(han)霖的国际化征程最亮眼的莫过于成功将产(chan)品足迹拓展至(zhi)全球50多个国家和(he)地区,全面覆盖(gai)亚(ya)洲、欧洲、美洲和(he)大洋洲,展现出强大的全球布局能力。
汉(han)利(li)康®、汉(han)曲优®、汉(han)斯状®等多款产(chan)品的海外(wai)市场拓展,不仅创造了多个“首(shou)个”或(huo)“最多”的行业纪录,更彰(zhang)显了复(fu)宏汉(han)霖的国际化实力。曲妥珠单抗汉(han)曲优®是首(shou)个中、美、欧三(san)地获批的生物类似药,成就了主(zhu)流监管(guan)市场的“大满贯”;H药汉(han)斯状®在印尼的成功上市,标志着其(qi)正式进军东南(nan)亚(ya)市场,也是首(shou)个登陆(lu)东南(nan)亚(ya)的国产(chan)PD-1,同时,其(qi)在日本市场的差(cha)异化布局以及欧盟获批的预(yu)期(qi),进一步巩固了复(fu)宏汉(han)霖在全球市场的地位;HLX14地舒单抗已提交(jiao)欧美新药上市注册申请,HLX11帕(pa)妥珠单抗提交(jiao)中美新药注册申请,更多国家的上市注册申报也在加速推进,更多新产(chan)品、新适应症的全球布局均取得突破性进展。
这些(xie)成功案例不仅验证了复(fu)宏汉(han)霖的国际化能力,更为其(qi)构筑了坚(jian)实的竞争壁垒。
首(shou)先,从全球产(chan)能与供应链角度(du)来看,复(fu)宏汉(han)霖实现了从“中国制(zhi)造”到“全球交(jiao)付”。
基于10余(yu)年的出海经验,复(fu)宏汉(han)霖已构建了全球化的临床、药政注册和(he)生产(chan)的全方位能力。公司建立了徐汇基地、松江基地(一)及松江基地(二)三(san)大生产(chan)基地,现有商业化总产(chan)能高达48,000升(sheng),实现全球产(chan)品常态化供应,全面覆盖(gai)中国、欧洲、拉丁美洲、中东北非、北美及东南(nan)亚(ya)等关键(jian)市场。同时,公司建立了一套符合国际质量标准的质量管(guan)理体(ti)系(xi),涵(han)盖(gai)从项目研发到物料管(guan)理、产(chan)品生产(chan)、质量控制(zhi)、产(chan)品供应链管(guan)理以及产(chan)品上市后跟踪的全生命周期(qi)。此前,公司商业化生产(chan)基地及配套的质量管(guan)理体(ti)系(xi)已通过中国国家药监局、欧洲药品管(guan)理局(EMA)、美国食药监局(FDA)、欧盟质量受权人(QP)以及国际商业合作伙伴的实地核查及审(shen)计,荣获中国、欧盟和(he)美国GMP认证。
H药在欧盟的获批,不仅是对其(qi)临床数据和(he)生产(chan)质量体(ti)系(xi)的国际认可,更为复(fu)宏汉(han)霖后续(xu)管(guan)线(如HLX22、HLX43等)的国际化进程铺平了道路,打开了市场对其(qi)创新药“出海溢价”的无限遐想。
其(qi)次,复(fu)宏汉(han)霖携手具有本地强大商业化网络和(he)资源的海外(wai)商业化合作伙伴,加速渗透(tou)当地市场,并考虑自建海外(wai)商业化团队(dui)。
在海外(wai)商业化方面,复(fu)宏汉(han)霖携手Abbot、Abbott、Accord、Dr. Reddy's、Eurofarma、Kalbe、Organon等跨国药企或(huo)当地龙头,高速推进产(chan)品在全球市场获批落地,凭借复(fu)宏汉(han)霖强大的产(chan)品研发及供应能力,以及合作伙伴在当地市场的资源,高效渗透(tou)主(zhu)流监管(guan)市场及新兴市场国家,夯实了对终端市场的掌控力。旗下产(chan)品已在北美洲、欧洲、拉丁美洲、东南(nan)亚(ya)、中东北非等区域实现上市销售。
据悉(xi),公司目前也在探索自建海外(wai)商业化团队(dui)和(he)更加灵活(huo)高效的出海模式。
最后,复(fu)宏汉(han)霖的创新平台也在加速全球化进程。
公司正在加速开发更多创新产(chan)品及潜在first-in-class适应症。同时,通过“国际多中心临床试验”加速管(guan)线国际化,如H药针对转移性结直肠癌(mCRC)的III期(qi)阶段临床已在日本、印尼等国家同步开展,有望成为全球首(shou)个针对不分型mCRC患者的一线免(mian)疫疗法。HLX22联合曲妥珠单抗的HER2双靶向疗法的国际多中心III期(qi)临床也已完成首(shou)例患者入组,有望成为同类疗法中首(shou)个用于治(zhi)疗HER2+胃癌的方案。这种“差(cha)异化适应症+国际多中心临床协同”的模式,将显著(zhu)提升(sheng)产(chan)品竞争格局,缩短创新药在全球市场的上市周期(qi)。
小结
2月以来,HLX11(帕(pa)妥珠单抗生物类似药)在美国获受理、H药在欧洲的获批、HLX15(达雷(lei)妥尤单抗生物类似药)超1.31亿美元授权欧美市场,一系(xi)列出海阔步,不仅再次印证了复(fu)宏汉(han)霖“生物类似药+生物创新药”双轮驱动发展的战略清醒,更是中国生物药企出海深化的生动写照。
通过“自主(zhu)研发+全球合作+自主(zhu)掌控”的三(san)重驱动,复(fu)宏汉(han)霖正逐步改写中国药企国际化的叙事(shi)篇章,从单纯的产(chan)品出口转向技术、产(chan)能、品牌的系(xi)统(tong)性输出。
展望未来,随着海外(wai)商业化团队(dui)的落地、更多研发管(guan)线的推进,复(fu)宏汉(han)霖有望成为少数真正具备全球竞争力的中国药企,为投资者带来见证“中国生物药”向“全球价值”跨越的历史性机遇。